细胞增殖和胚胎
减数分裂和受精作用与胚胎
减数分裂的过程
胚胎工程的理论基础
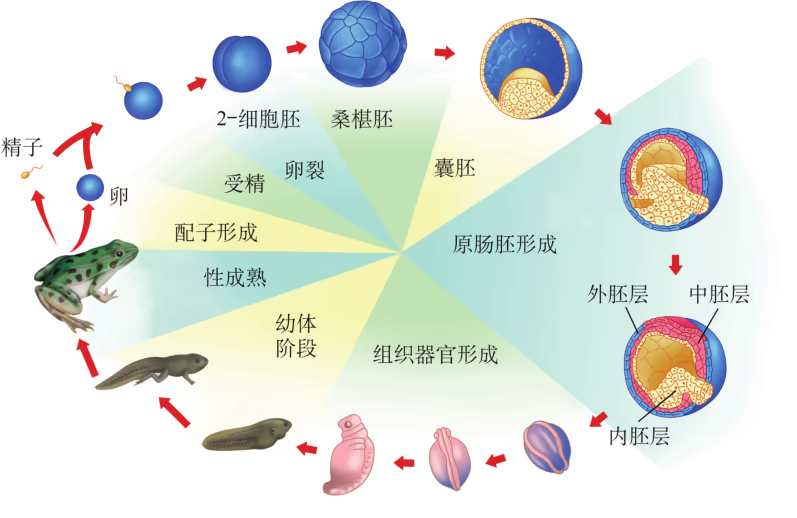
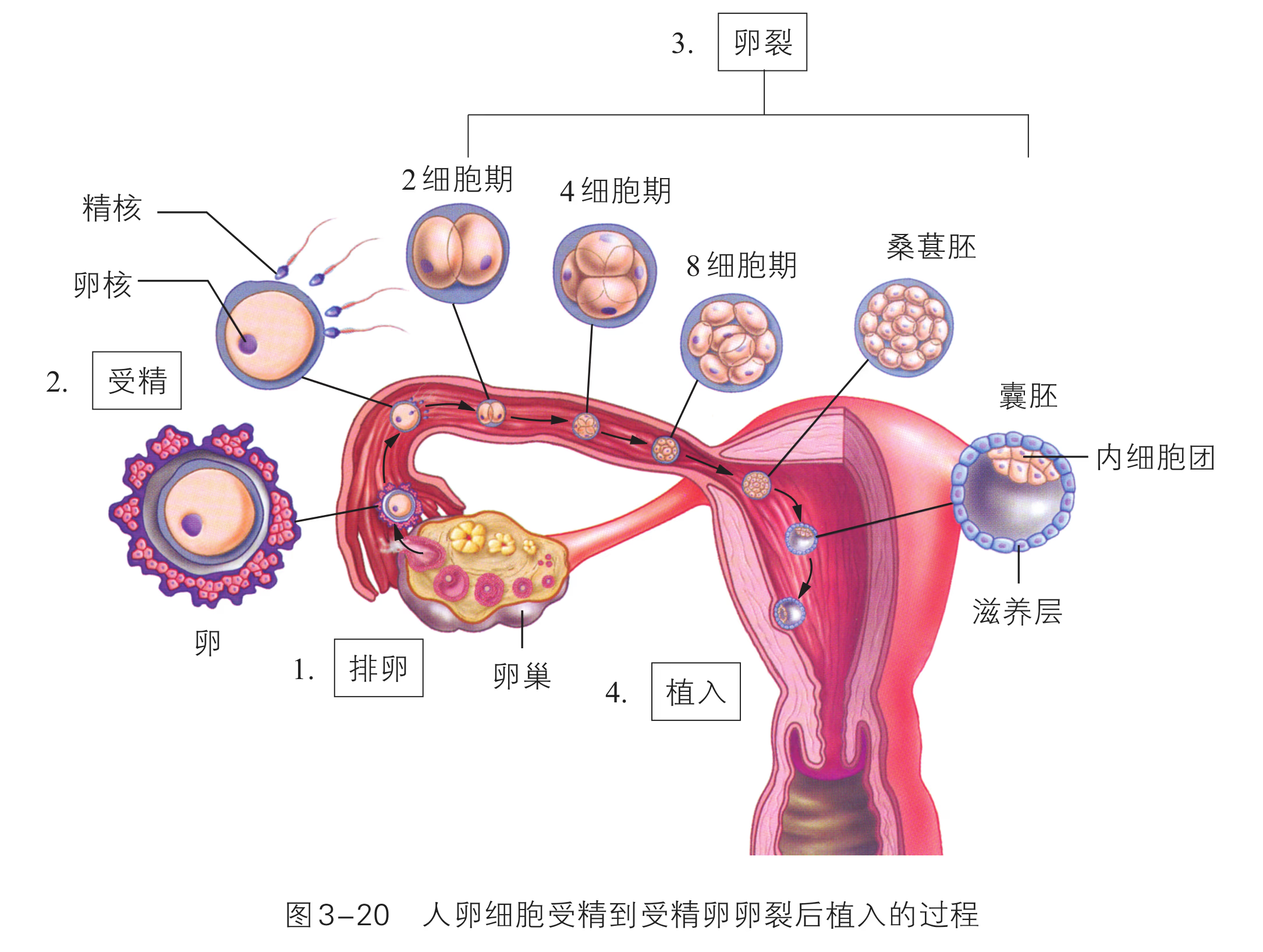
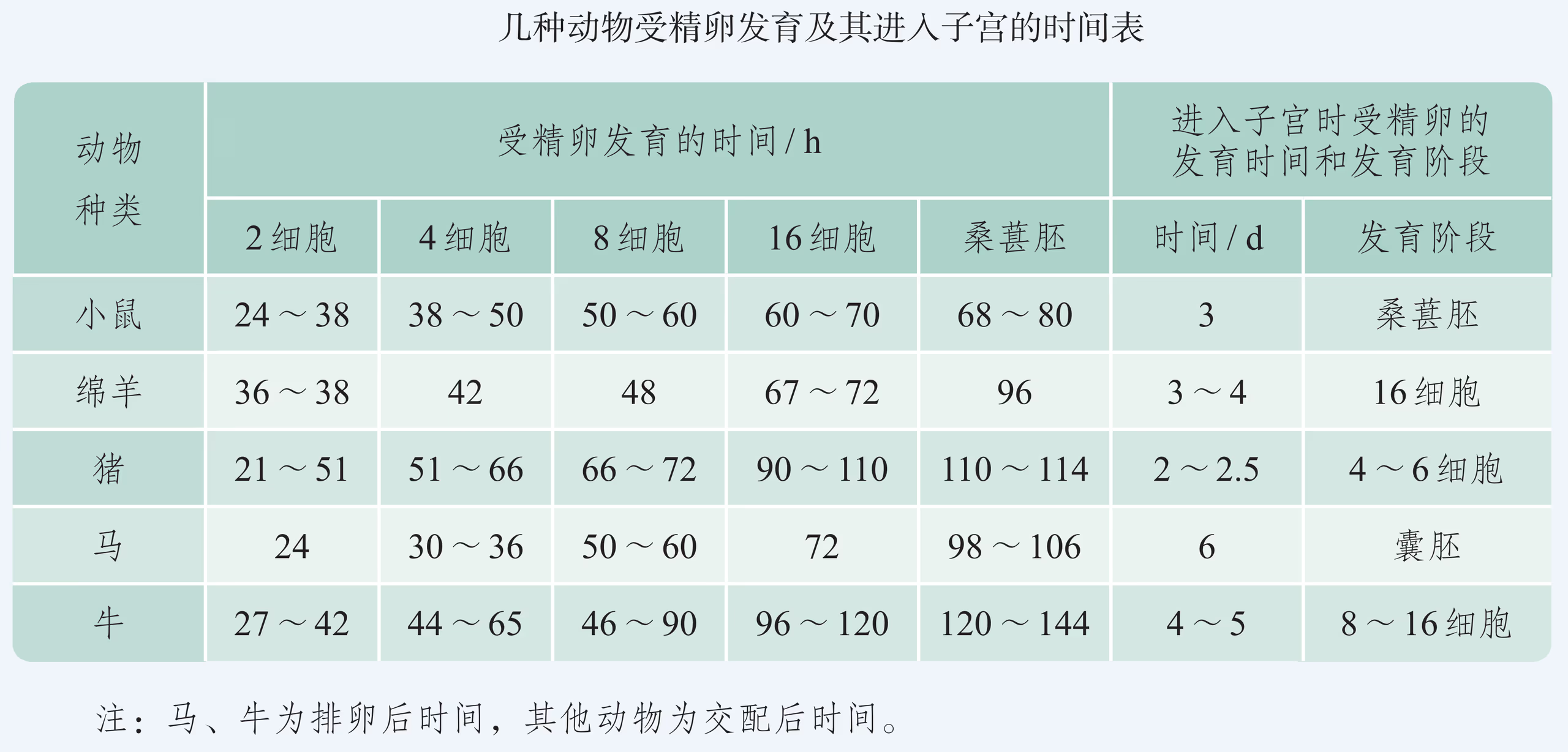
像培育试管婴儿这样,对动物早期胚胎或配子进行显微操作和处理以获得目标个体的技术称为胚胎工程。其操作的主要对象是生殖细胞、受精卵以及早期胚胎细胞。胚胎发育是胚胎工程的理论基础。那么,动物胚胎是如何发育的呢?虽然脊椎动物种类繁多,胚胎发育过程也存在差异,但其早期发育较为相似,分成受精、卵裂、桑椹胚、囊胚、原肠胚与器官形成等阶段(图 2-29)。
以蛙为例,由于卵黄分布不对称,精子与卵结合之后形成的受精卵分为动物极(发育为外胚层)和植物极(发育为中胚层和内胚层)。受精卵形成后开始卵裂,先分裂成两个细胞,之后细胞通常会逐次倍增,但胚胎的总体积大致不变。受精卵分裂成 16 \sim 32 个细胞的阶段,称为桑椹胚。在这个阶段,动物极细胞的分裂频率会超越靠近植物极且含有较多卵黄的细胞群,形成中空的球状胚,称为囊胚。随后形成的原肠胚具有外胚层、中胚层与内胚层,这三种胚层在之后会分化出各种组织和器官,逐渐发育成胚胎。
科学家通过模拟自然受孕的过程,逐渐洞悉胚胎发育的每一环节。这些都为胚胎工程(embryo engineering)的核心技术 — —体外受精(in vitro fertilization)和胚胎移植(embryo transfer)等技术的发展奠定了必要的基础,也促进了动物胚胎工程的迅猛发展,拓展了胚胎工程的应用领域。
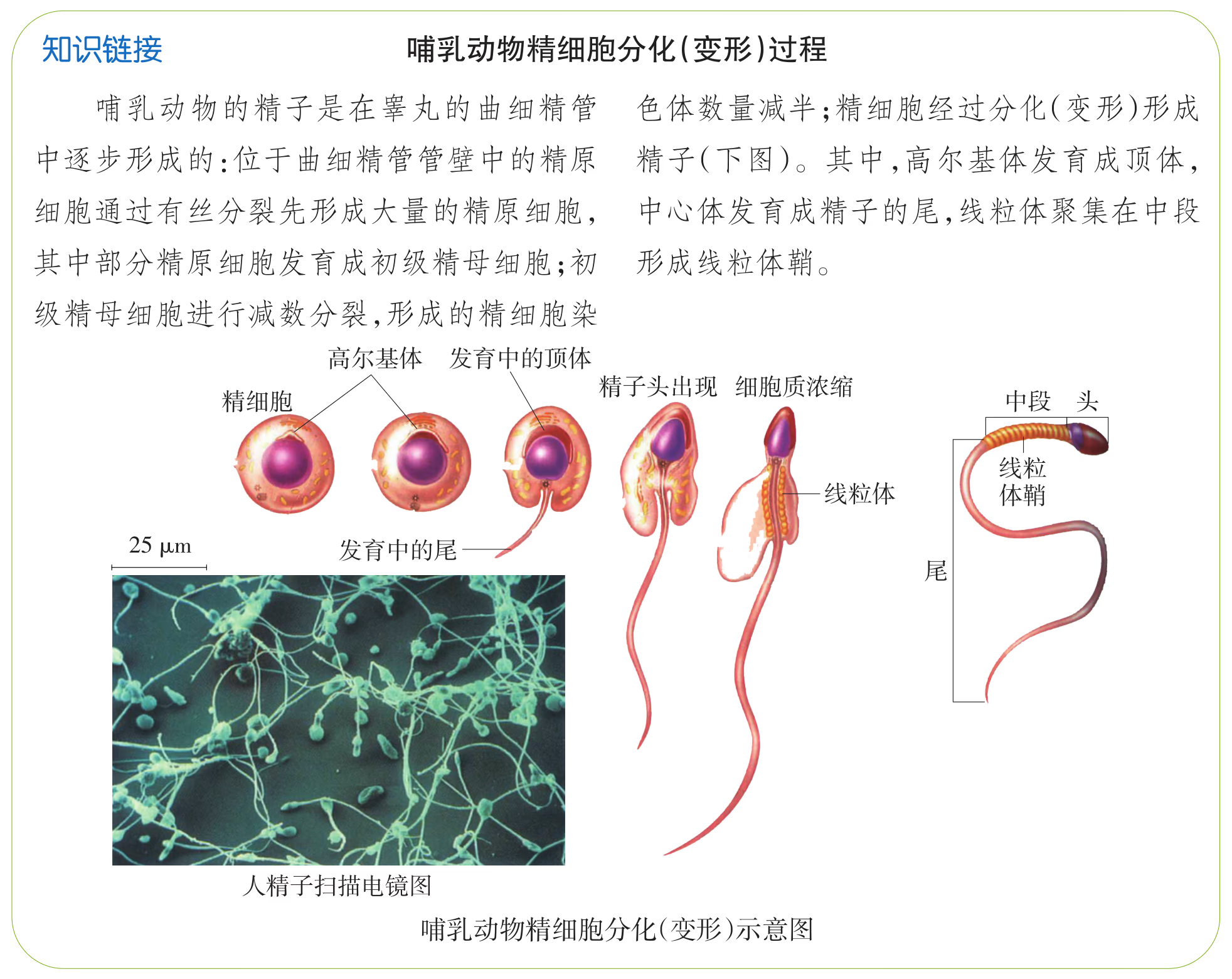
性成熟后,曲细精管内壁上的精原细胞形成初级精母细胞,每个初级精母细胞经过减数分裂形成 4 个精细胞,再经过分化(变形)过程形成精子,每个精子中都含有一个染色体组。精子的发生是依附在支持细胞上进行的,支持细胞为精子的发生提供营养,精子形成后进入曲细精管的管腔中。
哺乳动物卵细胞的发生是在雌性动物的卵巢中开始的。一个初级卵母细胞最终可能产生三个极体和一个卵细胞,它们的细胞中都含有一个染色体组。哺乳动物及其他许多脊椎动物的卵细胞发育在出生后会停止一段时间,直到雌性动物发育到性成熟期才继续发育。哺乳动物的初级卵母细胞经过减数分裂逐步形成成熟的卵子。减数第一次分裂是在排卵前完成的,排卵后,随着精子进入次级卵母细胞继续减数第二次分裂,一个次级卵母细胞分裂形成一个成熟的卵子和第二极体。雌、雄原核逐渐融合,形成受精卵。
当卵细胞质膜和透明带之间出现两个极体、雌雄原核融合时,表示受精作用已经完成,胚胎发育由此开始。哺乳动物的胚胎发育是指受精卵发育成幼体的过程,包括桑葚胚(morula)、囊胚(blastula)、原肠胚(gastrula)等主要发育阶段。
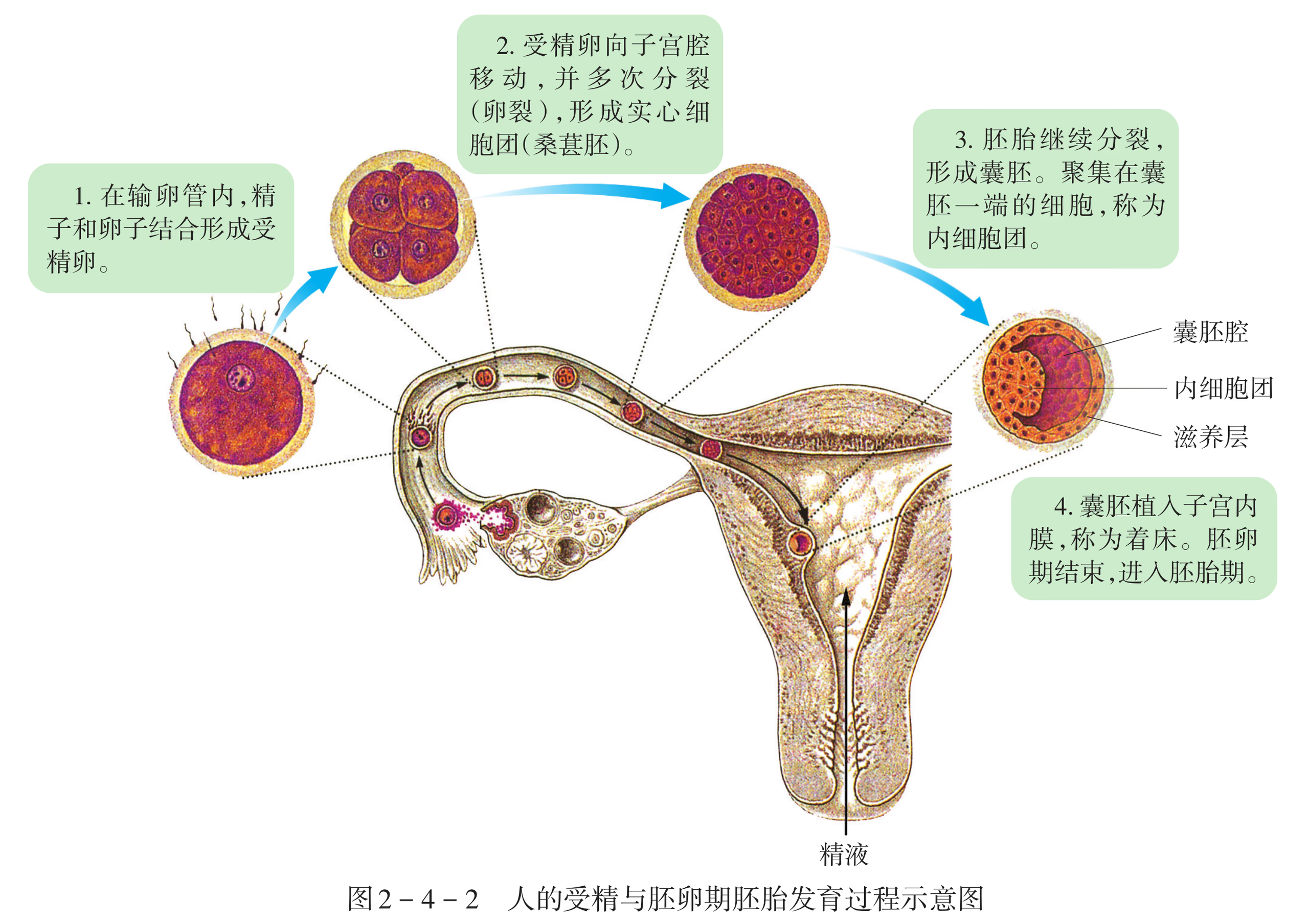
在人的胚胎发育中,受精卵一旦形成,便开始从输卵管移向子宫腔,在移动的同时,受精卵经过细胞分裂,形成囊胚并植入子宫内膜。从受精完成至第 1 周末为胚卵期。在这一时期,胚胎开始着床,囊胚进一步发育。
从第 2 周开始至第 8 周为胚胎期。囊胚植入子宫内膜过程中,囊胚壁逐渐发育为滋养层,内细胞团逐渐发育形成二胚层的胚盘,然后继续发育为三胚层的原肠胚。
从第 3 周开始,二胚层胚盘中的部分细胞增殖分化形成中胚层。随着三个胚层的分化,三胚层逐渐发育为各种器官的原基。胚盘发育为胚体,胚体凸入羊膜腔,浸泡在羊水中,胎盘逐渐形成。约在第 3 周末,心脏出现。
从第 4 周开始,三胚层逐渐发育,形成眼、耳、鼻等器官的原基;第 4 周末,神经系统开始发生;第 8 周末,各器官原基形成,胚体初具人形,胚胎期发育结束。
从第 9 周开始,进入胎儿期,各器官系统继续发育,多数器官逐渐出现不同程度的功能活动;从第 9 周到第 12 周,胎儿的头部仍占优势,躯体长高,脑部继续增长,眼睑闭合,眼内出现视网膜,从外生殖器可辨性别;从第 13 周到第 16 周,胎儿小脑变得突出,一般感觉器官分化,耳郭伸出,出现闭眼和吸吮的动作;从第 17 周到第 20 周,出现睫毛和眉毛,胎毛覆盖皮肤;21 周后,胎儿继续发育直至出生。
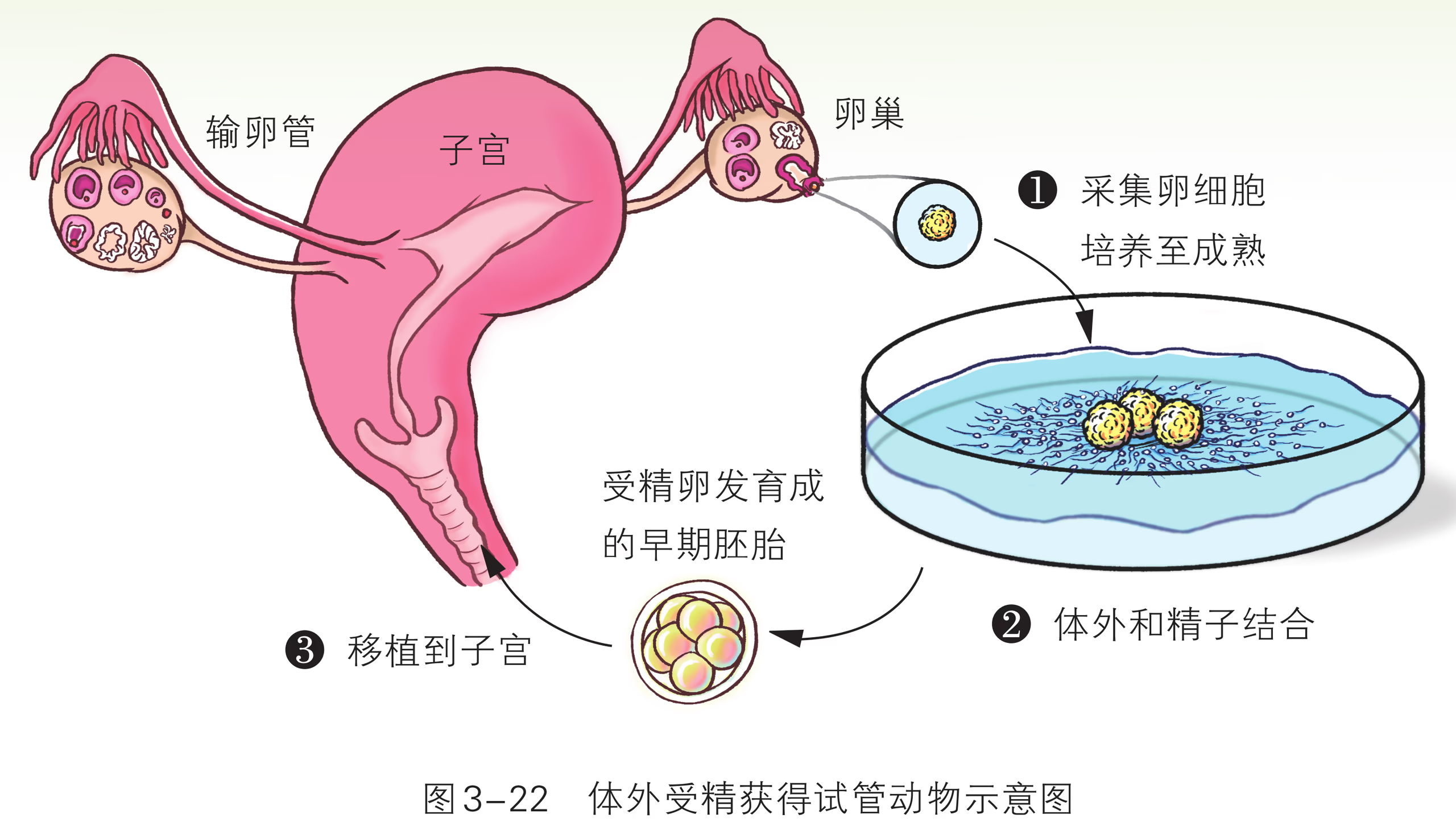
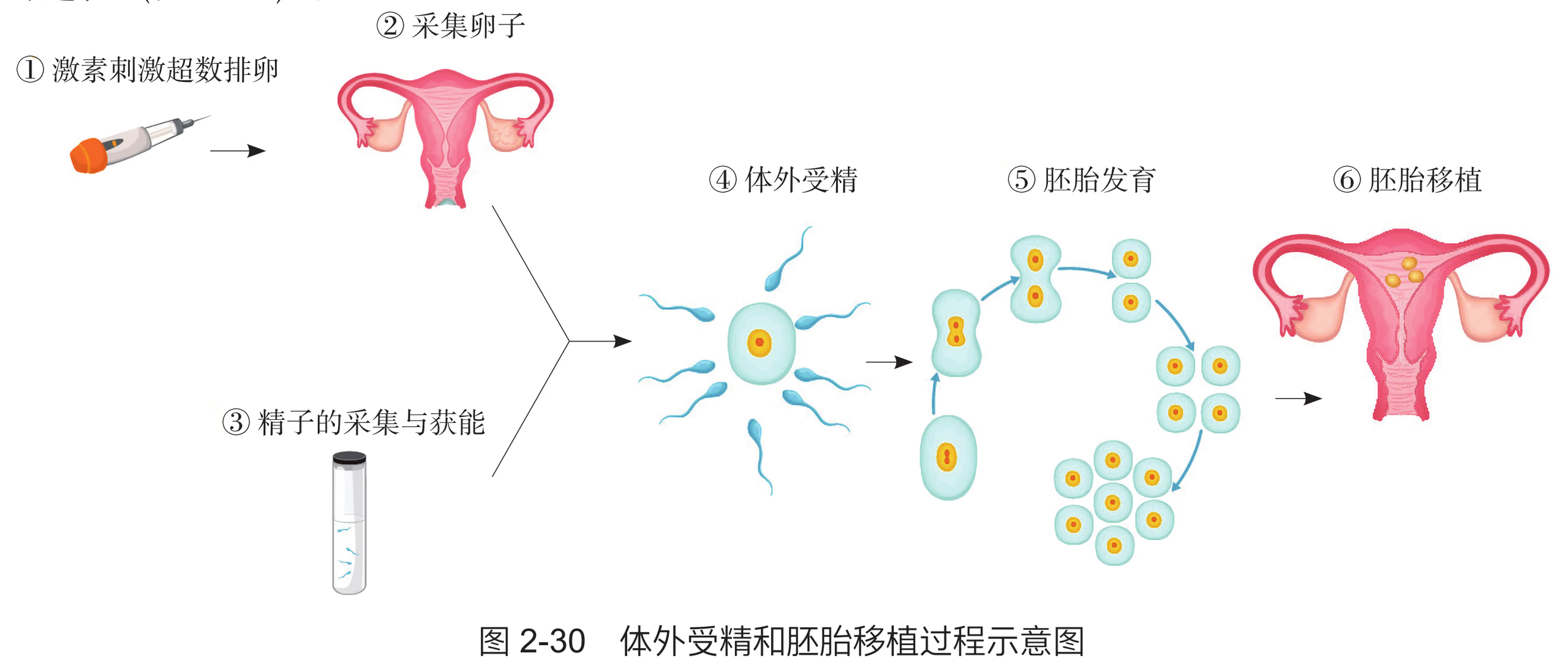
胚胎工程包括体外受精、胚胎移植、胚胎分割移植等技术。体外受精是指哺乳动物的精子和卵在人工控制的环境中完成受精过程的技术。这一技术主要包括卵的采集及成熟培养、精子的采集与体外获能、卵与精子的体外受精等环节。体外受精在动物优良品种的繁育中发挥着极为重要的作用。胚胎移植是将早期胚胎移植到同种且生理状态相同的受体动物体内,使之继续发育成为新个体的技术。胚胎移植实际上是产生胚胎的供体和孕育胚胎的受体分工合作、共同繁育后代的过程(图 2-30)。
胚胎工程的迅猛发展让人们大量繁殖优良家畜品种的愿望,正在成为现实。胚胎工程是指对生殖细胞、受精卵或早期胚胎细胞进行多种显微操作和处理,然后将获得的胚胎移植到雌性动物体内生产后代,以满足人类的各种需求。胚胎工程技术包括体外受精、胚胎移植和胚胎分割等。胚胎工程的许多技术,实际上是在体外条件下,对动物自然受精和早期胚胎发育条件进行的模拟操作。因此,了解哺乳动物受精和早期胚胎发育的规律十分重要。
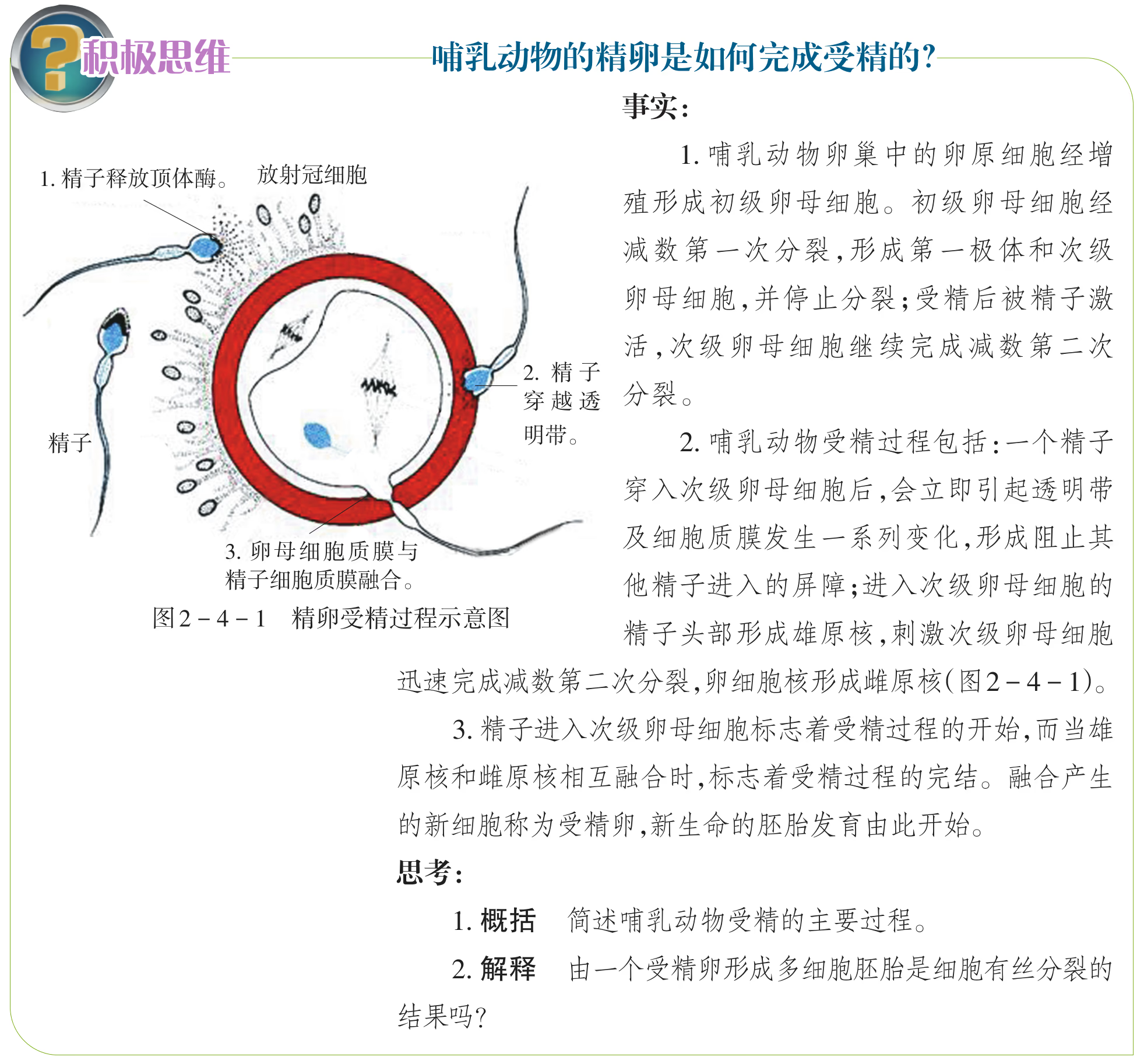
受精是精子与卵子结合形成合子(即受精卵)的过程,包括受精前的准备阶段和受精阶段。在自然条件下,哺乳动物的受精在输卵管内完成。
精子获能:科学研究发现,刚刚排出的精子不能立即与卵子受精,必须在雌性动物的生殖道发生相应的生理变化后,才能获得受精能力,这一生理现象称为“精子获能”。通过对精子获能机制的研究,科学家找到了使精子在体外获能的方法,实现了各种哺乳动物精子在体外条件下的获能,为体外受精技术的建立奠定了重要基础。使精子获能的方法有直接利用雌性动物的生殖道使精子获能;将精子培养在人工配制的获能液中使其获能等。获能液的成分因动物种类不同而有所差异,常见的有效成分有肝素、\ce{Ca^2+} 载体等。
卵子的准备:卵子一般在排出 \pu{2 \sim 3 h} 后才能被精子穿入。动物排出的卵子成熟程度不同,有的可能是初级卵母细胞,如马、犬等;有的可能是次级卵母细胞,如猪、羊等。但它们都要在输卵管内进一步成熟,到 M_{\text{II}} 期时,才具备与精子受精的能力。
受精阶段:获能后的精子与卵子相遇时,首先它释放出多种酶,以溶解卵细胞膜外的一些结构,同时借助自身的运动接触卵细胞膜。随之,精子的细胞膜与卵细胞膜融合,卵细胞膜外的透明带迅速发生生理反应,阻止后来的精子进入透明带。精子入卵后,卵细胞膜也会立即发生生理反应,拒绝其他精子再进入卵内。精子入卵后,尾部脱离,原有的核膜破裂并形成一个新的核膜,最后形成一个比原来精子的核还大的核,叫作雄原核。与此同时,精子入卵后被激活的卵子完成减数分裂Ⅱ,排出第二极体后,形成雌原核。雄、雌原核充分发育后,相向移动,彼此靠近,核膜消失。这个含有两个染色体组的合子就是受精卵。受精过程结束后,受精卵的发育也就开始了。
多数哺乳动物的第一极体不进行减数分裂Ⅱ,因而不会形成两个第二极体。在实际胚胎工程操作中,常以观察到两个极体或者雌、雄原核作为受精的标志。受精卵形成后即在输卵管内进行有丝分裂,开始发育。胚胎发育早期,有一段时间是在透明带内进行分裂,细胞的数量不断增加,但胚胎的总体积并不增加,这种受精卵的早期分裂称为卵裂。根据胚胎形态的变化,可将早期发育的胚胎分为以下几个阶段。
桑葚胚:当卵裂产生的子细胞逐渐形成致密的细胞团,形似桑葚时,这时的胚胎称为桑葚胚。
囊胚:胚胎进一步发育,细胞继续分化。聚集在胚胎一端的细胞形成内细胞团,将来发育成胎儿的各种组织;而沿透明带内壁扩展和排列的细胞,称为滋养层细胞,它们将来发育成胎膜和胎盘。
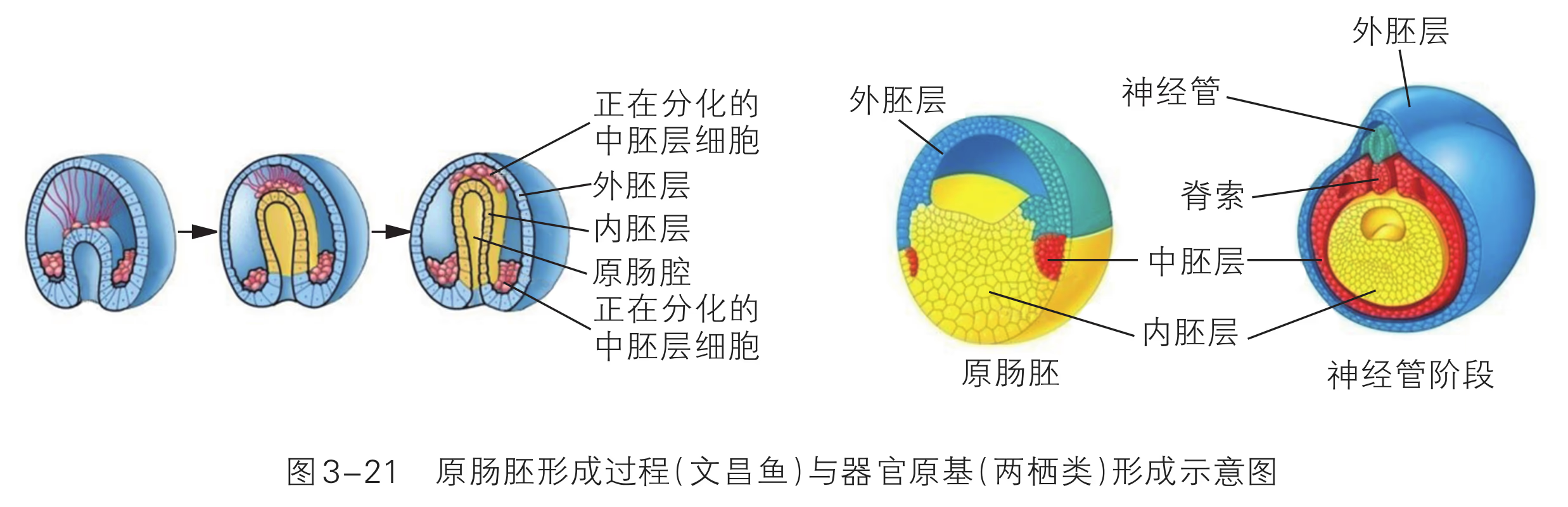
随着胚胎的进一步发育,胚胎的内部出现了含有液体的腔—囊胚腔,这个时期的胚胎叫作囊胚。囊胚进一步扩大,透明带破裂,胚胎从其中伸展出来,这一过程叫作孵化。孵化非常重要,如果不能正常孵化,胚胎就无法继续发育。囊胚孵化后,将发育形成原肠胚。原肠胚表面的细胞层为外胚层,向内迁移的细胞形成内胚层。随着发育的进行,一部分细胞还会在内、外两个胚层之间形成中胚层。这三个胚层将逐渐分化形成各种组织、器官等。
高等动物普遍的生殖方式是有性生殖,雌、雄生殖细胞结合成为受精卵标志着新生命的开始。鼠、牛和羊等哺乳动物的受精方式是体内受精,但新排出的精子不能立即使卵细胞受精,需要在雌性生殖道中发生一系列生理变化后,才具有受精能力,这一生理现象称为精子获能。获能后的精子耗氧量增加,迅速游向卵细胞并与之结合。精子的头部进入卵细胞后不久,精核就与卵核相遇,使彼此的 染色体会合在一起,形成受精卵。
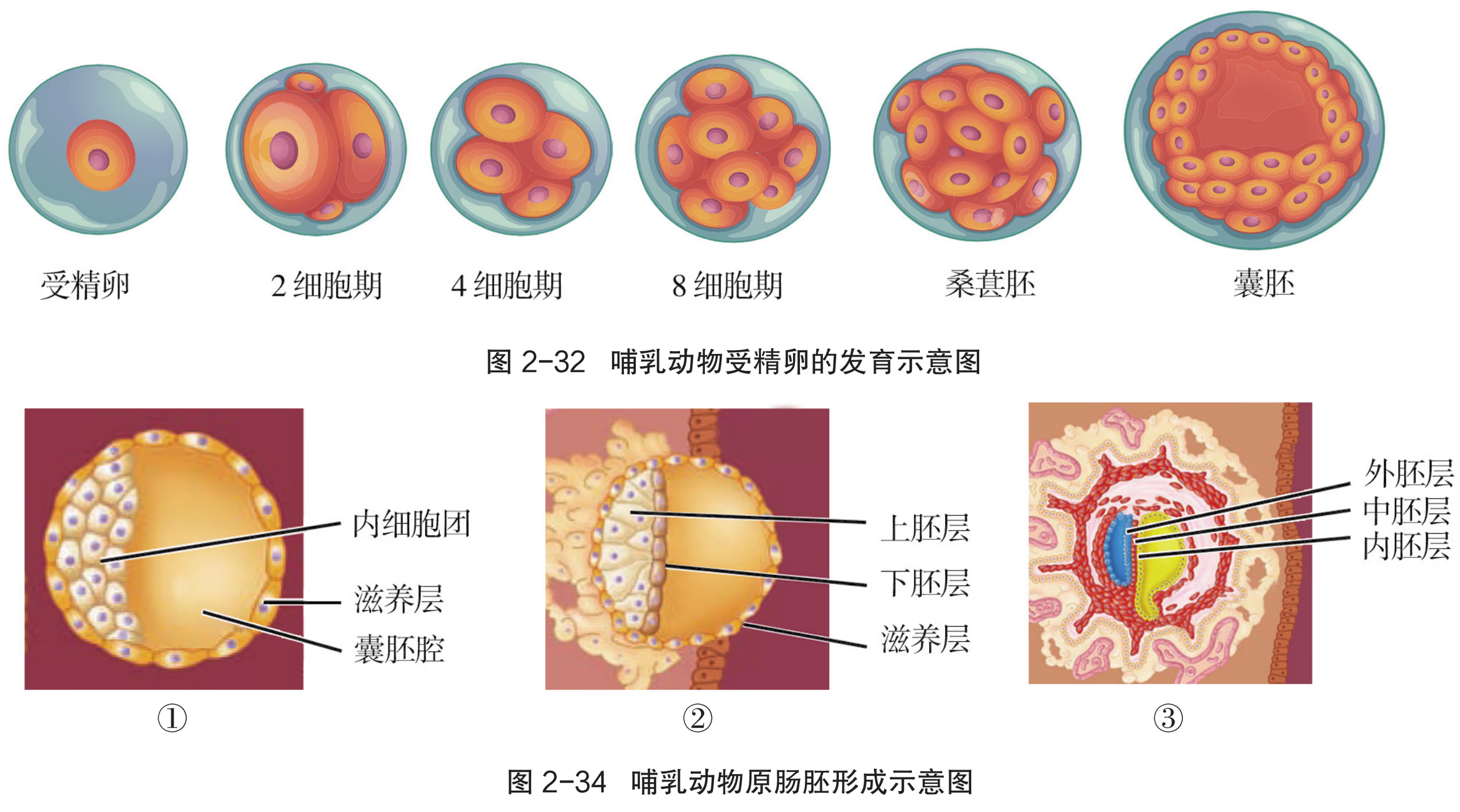
受精完成后,受精卵开始进行快速而有序的有丝分裂,这个过程叫作卵裂(cleavage)。由于卵裂期细胞分裂速度快,胚胎细胞来不及长大,下一次分裂就已开始,所以每个细胞越来越小,但胚胎总体积基本不变。当胚胎细胞达到 16~32 个左右时,形成了致密的细胞团,形似桑葚,叫作桑葚胚。
桑葚胚进一步分裂,胚胎内部形成空隙,逐渐发育成由内细胞团(inner cell mass)、滋养层细胞和囊胚腔构成的囊胚。囊胚中的内细胞团将发育成胎儿的各种组织,而滋养层细胞将发育成胎盘和胎膜。胚胎通过胎盘从母体中获得正常发育所需的氧气和营养物质等。
囊胚进一步发育,内细胞团的细胞不断分裂分化为 2 层细胞。靠近囊胚腔的一层细胞称为下胚层,位于下胚层和滋养层之间的细胞称为上胚层。上胚层的细胞继续分裂分化并迁入下胚层,逐渐置换了下胚层细胞,从而形成一层新细胞,称为内胚层。另一部分上胚层细胞继续分裂扩展,在上胚层和内胚层之间逐渐形成一层新细胞,称为中胚层。形成内胚层和中胚层之后,剩余的上胚层改称外胚层,这样就形成了由 3 个胚层构成的原肠胚。原肠胚的不同胚层之间相互作用,按各自的发育途径分裂和分化为相应的细胞和组织,为形成结构复杂的生命体奠定基础。
哺乳动物从受精卵到幼体的发育过程称为胚胎发育。根据胚胎形态的变化,早期胚胎的发育一般包括三个阶段:桑葚胚、囊胚和原肠胚。这些胚胎细胞还能像受精卵细胞一样发育成完整的个体吗?大量实验表明,在胚胎形成过程中,细胞的分化程度越高,全能性就越弱。尽管桑葚胚和囊胚的细胞在体积和数目上发生了很大变化,但是细胞的功能和发育潜能基本没有改变,分离开来的细胞团仍然可以独立发育成个体。而原肠胚的细胞由于分化程度较高,分割开的胚胎已经不能各自发育成一个新个体。胚胎形成过程中的这些特征为科学家对早期胚胎进行干预和改造提供了可能性。
胚胎分割技术
1942 年,科学家成功地对大鼠二细胞胚胎进行了分离和培养。后来,一些科学家尝试着把绵羊八细胞胚胎分割成 4 份,每份 2 个细胞,再将它们植入母羊子宫内,结果母羊成功地产下 4 只小羊。像这样,用机械方法将早期胚胎平均分割成二分胚、四分胚甚至八分胚,经培养后植入受体,以得到同卵双生或同卵多生后代的技术称为胚胎分割(embryo bisection)技术。这种技术被视为一种胚胎克隆方法。 胚胎分割常需要利用显微操作仪进行操作。在操作时,应选择形态正常、发育良好的桑葚胚或囊胚,在盛有操作液(含有质量分数为 10\% \sim 20\% 的血清)的培养皿中用分割针或分割刀片将胚胎切开。如果切割的是囊胚,一定要均等分割内细胞团;然后再将吸出的半个胚胎注入一个已经清空的透明带中或直接将其移植到受体中。
- 显微针分割法 该法适用于卵裂球阶段的胚胎。操作时在显微操作仪下将胚胎固定,用显微针在透明带上做一切口,将卵裂球从透明带中移出,并吹吸卵裂球使之离散,将其装入 2 个预先准备好的空透明带内,进行移植。该方法具有较高的同卵双生率,但操作程序复杂。
- 显微刀分割法 该法适用于对桑葚胚和早期囊胚进行分割。在显微操作仪下固定胚胎,用显微刀片将胚胎均匀地一分为二,分别装入空透明带中,进行移植。
- 酶软化透明带后显微分割法 用质量分数为 0.5\% 的链霉蛋白酶溶液软化胚胎透明带。若是紧密化胚胎(如桑葚胚),则需在无钙、无镁的平衡盐溶液中处理 \pu{20 min},使胚胎去紧密化。将胚胎固定,把针置于欲分割的胚胎上面,使其与胚胎呈 \pu{30 ^{\circ}},对准胚胎的正中平分线徐余下压,即可将一个胚胎分割成两半。
- 酶消去透明带后显微分割法 用质量分数为 0.25\% \sim 0.5\% 的链霉蛋白酶溶液消去胚胎透明带,然后用显微针或显微刀将裸胚一分为二。
胚胎分割技术不仅能使可供胚胎移植的胚胎数目成倍增加,而且可以产生遗传性能相同的后代。这对畜牧业生产和科学研究都有重要价值。例如,正常情况下,一头良种奶牛一生约可产犊 10 头,如用胚胎分割技术进行胚胎分割并移植到其他用作“寄母”的普通母牛子宫内,就可以获得大量的良种奶牛。在实际应用中,胚胎分割以二分胚的移植成功率最高。我国相继对猪、牛、马、绵羊、山羊、家兔和小鼠等动物进行了二分胚分割(图 2-4-6),并应用到胚胎移植中。
在动物研究的基础上,英国学者爱德华兹(R. Edwards)和斯特普托(C. Steptoe)最早开展了人类体外受精和胚胎移植技术的研究。1977 年,他们利用腹腔镜取卵,完成体外受精,并在受精卵发育到 8 细胞胚胎阶段移植入母体子宫内获得妊娠。1978 年 7 月,在英国剑桥大学诞生了世界首例“试管婴儿”。我国首例试管婴儿于 1985 年 4 月诞生于台湾。此后,人类的体外受精和胚胎移植技术得到了进一步的发展和应用,为部分生育困难患者带来了福音。
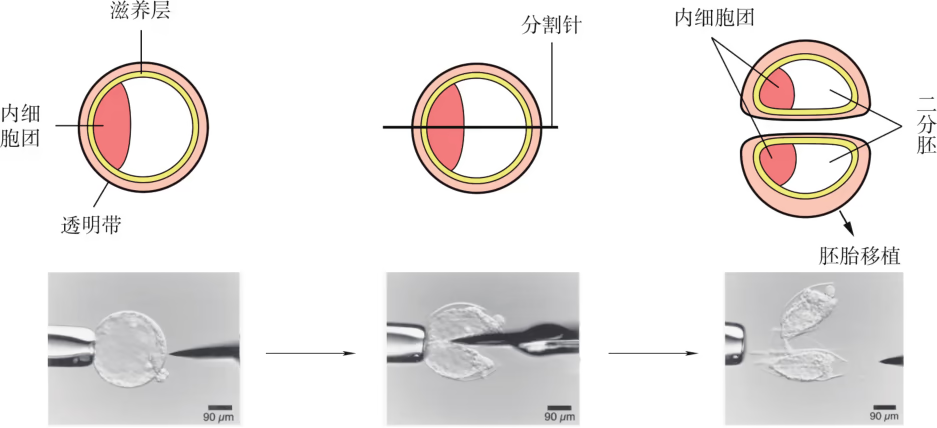
胚胎分割移植是将一枚胚胎用显微手术的方法分割成几份,经体内或体外培养,然后移植入受体中,以得到同卵双生或同卵多生后代的技术。进行胚胎分割时,应选择发育良好、形态正常的桑椹胚或囊胚,将其移入盛有操作液的培养皿中,在显微镜下用分割针或分割刀进行分割。在对囊胚阶段的胚胎进行分割时,还要特别注意将内细胞团均等分割(图 2-31),否则会影响分割后胚胎的恢复和进一步发育。
科学家们首先进行了大鼠卵裂球的分离和培养,随后又以小鼠为实验对象,获得了世界首例半胚来源的活体动物。经过多年的发展,胚胎分割移植在理论和技术方法上都已较为完善,尤其是对牛、羊等大型经济动物实施胚胎分割移植技术,可增加胚胎移植中的有效胚胎数、提高妊娠率,从而增加后代数量。与细胞核移植技术相比,胚胎分割移植具有更高的成功率。
胚胎分割:早期胚胎细胞具有很强的分裂能力,并保持着细胞全能性,能不能将一个胚胎分割成几份,从而提高胚胎的利用率?基于这样的设想,胚胎分割技术逐渐发展成熟。胚胎分割是指采用机械方法将早期胚胎切割成 2 等份、4 等份或 8 等份等,经移植获得同卵双胎或多胎的技术。来自同一胚胎的后代具有相同的遗传物质,因此胚胎分割可以看作动物无性繁殖或克隆的方法之一。胚胎分割所需要的主要仪器设备为体视显微镜和显微操作仪。在进行胚胎分割时,应选择发育良好、形态正常的桑葚胚或囊胚,将它移入盛有操作液的培养皿中,然后在显微镜下用分割针或分割刀分割。在分割囊胚阶段的胚胎时,要注意将内细胞团均等分割。对于不同发育阶段的胚胎,分割的具体操作不完全相同。分割后的胚胎可以直接移植给受体,或经体外培养后,再移植给受体。经过 40 多年的发展,胚胎分割技术日趋成熟。这项技术可以促进优良动物品种的繁殖,产生的遗传性状相同的后代是进行遗传学研究的宝贵材料。此外,在胚胎移植前,进行性别鉴定、遗传病筛查等,对于人工控制动物性别、动物繁育健康后代具有重要意义。
1978 年,科学家将小鼠的桑葚胚一分为二,获得了成功。1979 年,科学家分割绵羊胚胎获得了同卵羔羊。20 世纪 80 年代后,人们建立了系统的胚胎分割方法,并相继得到 1/4 和 1/8 分割胚胎的后代。我国的胚胎工程专家也进行了分割胚胎移植的实验研究,成功地对小鼠、家兔、绵羊、山羊和牛等动物进行了分割胚胎移植,并将二分胚胎分割技术应用到牛和羊的胚胎移植中。尽管胚胎分割技术已经在多种动物中取得成功,但仍存在一些问题,如刚出生的动物体重偏低,毛色和斑纹可能存在差异等。实践证明,采用胚胎分割技术产生同卵多胚的可能性是有限的,分割次数越多,分割后胚胎成活的概率越小。目前,仍然以二分胚胎的分割和移植效率最高,这成为提高家畜胚胎利用率的手段之一。
胚胎移植技术
胚胎工程是指对动物的胚胎进行人为操作和处理以获得目标个体的技术,包括体外受精、胚胎移植和胚胎分割等现代生物技术。精子和卵母细胞结合后,将受精卵移入相应的培养液中培养。培养液的基本成分包括维生素、氨基酸、蛋白质、无机盐和糖类等。待培养的胚胎发育到特定阶段后,再进行移植。像这样将良种雌性动物配种后,从其生殖道取出早期胚胎或通过体外受精及其他方式(如转基因、核移植)得到的受精卵或胚胎,再移植到同种的同时发情排卵但未经配种的其他雌性动物的体内,使它们进一步发育为新个体的技术,称为胚胎移植技术。
19 世纪末,科学家当时以兔为实验对象成功地完成了哺乳动物的胚胎移植。20 世纪 30 \sim 70 年代,胚胎移植成为当时生物学研究的主要方向之一,在多种家畜如绵羊、山羊、猪、牛和马上相继获得成功。20 世纪 60 年代后,科学家开始采用激素对供体进行超数排卵处理,并对受体进行同期发情处理。此后,胚胎移植技术发展迅猛,成为畜牧业中广泛使用的一种技术。胚胎移植实际上是产生胚胎的供体和孕育胚胎的受体共同繁殖后代的过程。这一技术又被形象地称为“借腹怀胎”。动物胚胎移植过程一般分为供体和受体的选择、供体和受体同期发情处理、供体的超数排卵处理和受精、胚胎收集以及胚胎移植。
胚胎移植作为胚胎工程中的一项技术具有重要的应用价值。例如,胚胎移植能发挥优良母畜的繁殖能力,迅速扩大优良畜种数量,加速优良畜种的推广应用;能缩短世代间隔,提高家畜改良速度;能长期保存冷冻胚胎,便于优良品种的种质运输和保存。同样,胚胎移植也使胚胎分割和核移植等技术成为基础生物学研究的重要手段。
胚胎移植是指将通过体外受精及其他方式得到的胚胎,移植到同种的、生理状态相同的雌性动物体内,使之继续发育为新个体的技术。其中提供胚胎的个体称为“供体”,接受胚胎的个体叫“受体”。通过任何一项技术(如转基因、核移植和体外受精等)获得的胚胎,都必须移植给受体才能获得后代。以牛的胚胎移植为例,胚胎移植主要包括供体、受体的选择和处理,配种或人工授精,胚胎的收集、检查、培养或保存,胚胎的移植,以及移植后的检查等步骤。
进行胚胎移植的优势是可以充分发挥雌性优良个体的繁殖潜力。在这项技术中,供体的主要职能变为产生具有优良遗传特性的胚胎,繁重而漫长的妊娠和育仔任务由受体取代,这就大大缩短了供体本身的繁殖周期。同时,在对供体施行超数排卵处理后,可获得多枚胚胎,经移植可得到多个后代,这使供体的后代数是自然繁殖的十几倍到几十倍。超数排卵是指应用外源促性腺激素,诱发卵巢排出比自然情况下更多的成熟卵子。
体外受精技术
通过人工操作使卵子在体外受精,经培养发育为早期胚胎后,再进行移植产生的个体。体外受精技术是提高动物繁殖能力的有效措施,还可以为胚胎移植提供可用的胚胎。在这个过程中,首先要做的就是体外受精。哺乳动物的体外受精技术主要包括卵母细胞的采集、精子的获取和受精等步骤。采集到的卵母细胞和精子,要分别在体外进行成熟培养和获能处理,然后才能用于体外受精。一般情况下,可以将获能的精子和培养成熟的卵子置于适当的培养液中共同培养一段时间,来促使它们完成受精。
采集一定发育阶段的精子和卵母细胞是实施体外受精技术的重要环节。 体外受精技术是指哺乳动物的精子和卵子在体外人工控制的环境中完成受精过程的技术。其基本原理是人工模拟体内环境,包括营养、温度、\pH 等,促使卵母细胞成熟,同时使精子获能,最终完成受精作用等。这项技术现已日趋成熟,成为一项重要而常规的动物繁殖技术。体外受精技术包括采集精子、采集卵母细胞和体外受精等主要步骤。
采集精子 采集动物精子的方法主要是假阴道法。假阴道通过模仿发情的雌性动物在交配时阴道的压力、温度和润滑度等条件,创造了适合采精的环境。采精者可手持假阴道,利用假台畜让被采精动物在模拟交配时将精液射入假阴道内,从而达到采集精子的目的。 采集的精子可以立即使用或冷冻保存待用。由于精液中含有精子获能的抑制因子,冷冻液中还含有防冻剂等成分,精液中含有一定量的死精子,一般需要分离并获取有活力的精子。
采集卵母细胞 采集卵母细胞的方法主要有抽吸法、机械破碎法等。 采集较大型的动物如牛、猪的卵母细胞时,一般采用抽吸法。这是一种从活体卵巢中采集卵母细胞时的常用方法。技术人员操作时借助超声波探测仪和内窥镜等进行,将注射器针头刺入卵泡中一并吸出卵泡液和卵母细胞,再在显微镜下进行筛选。该方法的优点是可以有目的地选择卵泡,分离得到适当成熟程度的卵母细胞。活体采卵对于充分发挥优良母畜的繁殖潜力具有一定意义。 采集较小型的动物如小鼠、兔的卵母细胞时,一般采用机械破碎法。这是一种从宰杀后的雌性动物卵巢上采集卵母细胞的方法。技术人员操作时,将刚宰杀的雌性动物体内摘出的卵巢置于培养皿中,用针头刺破卵巢和卵泡,再在显微镜下对卵母细胞进行筛选。该方法的优点是可以得到各种成熟程度的卵母细胞,缺点是在刺破卵巢和卵泡的过程中有可能刺伤卵母细胞。对于较小型的动物,还可以采用促性腺激素处理的方法,使其超数排卵,这样获得的卵母细胞可以直接与获能后的精子进行体外受精。 如果采集到的卵母细胞尚未成熟,需通过体外培养使之成熟。经过体外培养后,一般要通过相关的形态观察指标(如 \pu{7 d} 后的囊胚发育率)对卵母细胞的体外成熟情况进行评价。
人卵泡的发育 人卵泡的形成和在卵巢中的储备是在胎儿期完成的。人的胚胎性别分化后,雌性胎儿卵巢内的卵原细胞经过有丝分裂增加其数量,其中部分卵原细胞发育为初级卵母细胞。由于它们被卵泡细胞所包围,一般称之为卵泡。 新生儿(女性)出生时卵巢内约有 15 万 \sim 50 万个卵泡。青春期以后,卵泡逐渐减少,女性一般只有 300 \sim 400 个卵泡能发育成熟,其余卵泡均发育到一定程度即自行退化。 有些哺乳动物和人一样,卵泡的发育也始于胚胎时期。一般认为,哺乳动物出生后卵巢内卵泡不可更新,但仍有科学家在不断研究卵巢中是否存在生殖干细胞。这可能对生殖医学以及干细胞研究等具有深远意义。
体外受精 哺乳动物的交配往往发生于发情的开始或发情盛期,排卵则发生于发情结束前后,这既保证了精子能先于卵母细胞到达受精部位,也给精子留了充足的获能时间。精子获能后发生膜流动性的增加、膜对 \ce{Ca^2+} 通透性提高、胞内环磷酸腺苷(cAMP)浓度的升高、表面电荷降低以及游动方式等一系列变化,其重要意义在于增强了精子的代谢能力和运动能力。 获能后的精子会引起 \ce{Ca^2+} 内流到精子内,同时伴随精子细胞质膜通透性的改变和胞内 \pH 升高,刺激顶体反应的发生。顶体反应主要发生在精子头部。精子与卵子利用各自表面的特异性蛋白进行识别后,发生特异性结合。精子头部前端与卵母细胞透明带接触后,顶体外膜与精子头部的细胞质膜融合,顶体破裂释放出的顶体酶溶解卵母细胞周围的放射冠和透明带,精子即可穿过透明带到达卵母细胞表面。随着精子进入卵母细胞,雄原核与雌原核融合,最终形成受精卵。
家兔、猪等动物的精子,放入人工配制的获能液中,经培养即可获能;牛、羊等动物的精子,可放入一定浓度的肝素或相应的 \ce{Ca^2+} 载体溶液中,诱导精子获能。 在人为控制的适宜条件下和专用的受精溶液中,获能的精子和培养成熟的卵母细胞放在一起培养一段时间,可以在体外完成受精过程。
日趋成熟的体外受精技术可用于研究哺乳动物生殖细胞的发生、受精和早期胚胎发育机制等。在家畜品种改良探索过程中,体外受精技术为胚胎生产提供了经济而高效的方法,对充分利用优良种质资源、缩短家畜繁殖周期、加快品种改良速度等具有重要价值。