硼族元素概述
铝单质
铝单质概况
铝是地壳中含量最高的金属,大多以化合态存在。铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物。
铝土矿是最重要的一种铝矿石,其主要成分为 \ce{Al2O3}(也以氢氧化铝形式存在),其中还含有针铁矿、赤铁矿、高岭土(含二氧化硅)和少量的二氧化钛。
三氧化二铝同时为绿宝石和蓝宝石的主要成分。
纯铝的硬度和强度较小,不适合制造机器零件等。向铝中加入少量合金元素,可制成铝合金。铝合金是目前用途广泛的合金之一。
硬铝中含铜、镁、锰、硅,它的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
铝的化学性质
还原性:
氧化剂 反应方程式 \ce{O2} \ce{4Al + 3O2 -> 2Al2O3} \ce{Cl2} \ce{2Al + 3Cl2 -> 2AlCl3} \ce{S} \ce{2Al + 3S -> Al2S3} 其中三氯化二铝于水发生双水解,生成 \ce{Al(OH)3,H2S}。
与酸减和水的反应:
与浓硫酸、浓硝酸:生成致密氧化膜 \ce{Al2O3},钝化。
与非氧化性酸(仅强酸):\ce{2Al + 6H+ -> 2Al^3+ + 3H2 ^}。
与碱(仅强碱):\ce{2Al + 2OH- + 6H2O -> 2[Al(OH)4]- + 3H2}。
铝的金属性不强,非金属性也不强,因此之和强酸强碱发生反应。
毛刷实验:
\ce{2Al + 3Hg^2+ -> 2Al^3+ + 3Hg}。
铝溶解在汞中,生成铝汞剂(铝的汞溶液)。
铝盐的水解:
\ce{Al2S3 + 6H2O = 2Al(OH)3 v + 3H2S ^}
泡沫灭火器
\ce{Al^3+ + 3HCO3^- = Al(OH)3 v + 3CO2 ^}
铝的工业制取
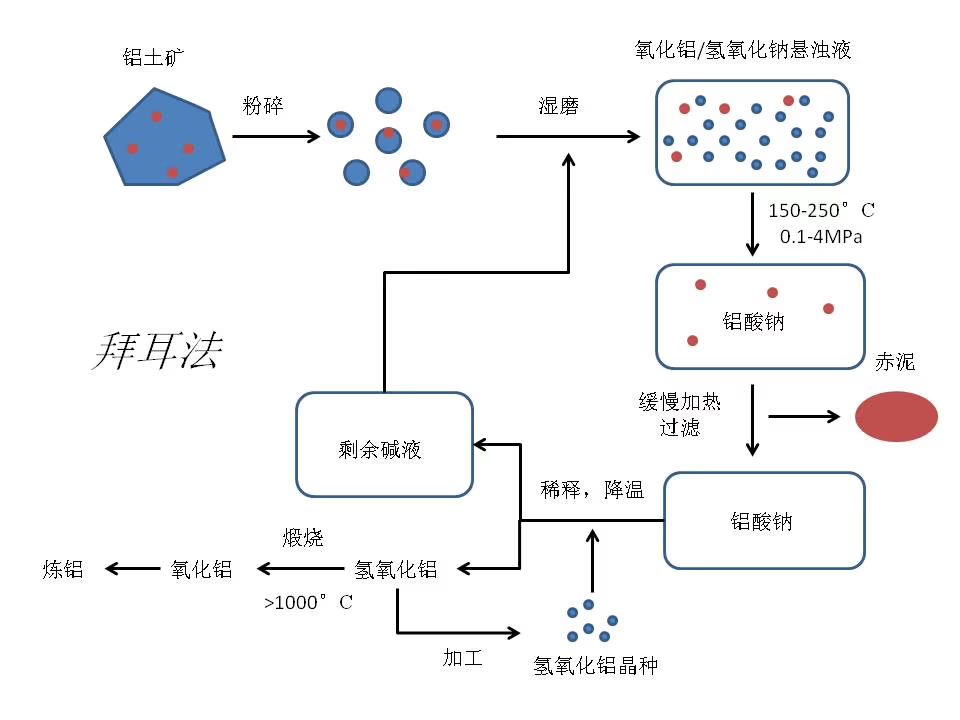
常见的工业制铝为霍尔-埃鲁法,现在常与与拜耳法联用,产铝量大。
粉碎:
用水冲洗掉颗粒表面的粘土等杂质。
将洗净的固体与低浓度氢氧化钠(拜耳法余液)相混合,借助球磨形成悬浊液。
随着粒径逐渐变小,铝土矿的比表面积大大增加,这有助于加快后续化学反应的速度。
溶出:
铝土矿和高浓度氢氧化钠溶液形成的悬浮液随后进入反应釜,通过提高温度和压力使铝土矿中的氧化铝和氢氧化钠反应,生成可以溶解的偏铝酸钠(\ce{Na[Al(OH)4]})。
在和氢氧化钠反应时,铝土矿中所含的铁的各种氧化物、氧化钙和二氧化钛基本不会和氢氧化钠反应,形成了固体沉淀,留在反应釜底部,它们会被过滤掉,形成的滤渣呈红色,被称作赤泥,拜耳法会导致部分氢氧化钠进入赤泥,给赤泥带来了强腐蚀性,其 pH 可以达到 11\sim12,这带来了严重的环境问题。
而铝土矿中含有的二氧化硅杂质则会和氢氧化钠反应,生成同样溶于水的硅酸钠,为了除去硅酸钠,缓慢加热溶液,促使二氧化硅、氧化铝和氢氧化钠生成方钠石结构的水合铝硅酸钠,沉淀下来,然后过滤除掉,这样一来,就只有铝酸钠留在上清液中。
析出:
热的溶液进入冷却装置中,加水稀释同时逐渐冷却,铝酸钠会发生水解,生成氢氧化铝,此时加入纯的氧化铝粉末作为晶种,会析出白色的氢氧化铝固体。
有的厂家对这一步进行了改进,通入过量二氧化碳帮助产生氢氧化铝。
过滤掉生成的氢氧化铝后,剩余的浓度仍然较高的氢氧化钠溶液会循环利用,用于处理另一批铝土矿,溶出氢氧化铝。
分解:
已经生产出的氢氧化铝则在 \pu{1000°^oC} 以上煅烧,可以分解成氧化铝。
具体煅烧温度依据所需氧化铝的晶型和粒径来决定,生产的氧化铝随后可通过霍尔-埃鲁法电解制取金属铝。
电解:
熔融氯化铝不导电,因此工业中常用电解熔融氧化铝。
霍尔-埃鲁法是电解氧化铝和冰晶石(主要成分是 \ce{Na3AlF6} 六氟合铝酸钠)的熔融混合物制取铝的化工过程。
\ce{2Al2O3(熔融) ->[通电][冰晶石] 4Al + 3O2 ^}
由于氧化铝的熔点超过 \pu{2000°^oC},电解过程所需的热力和电力成本过高,无法投入实际应用。氧化铝与冰晶石的混合物的熔点降到大约 \pu{1000°^oC},有时候会加入氟化铝以进一步降低熔点。
冰晶石的加入,一方面可以降低熔点,另一方面也可以改变电解进程,但其具体作用机理还不完全清楚。
在阳极,
阳极上生成二氧化碳的反应是放热的,放出的热量可以补充一部分用于熔融的能量;霍尔—埃鲁法所用的电解池通常使用的电流都达数百安培,电阻的存在又需要多余的能量。
电解池中的温度通过电阻元件控制,石墨阳极的氧化增加了电流的效率。虽然室温下固态的冰晶石比固态铝密度要大,而在1000°C左右,铝的密度(大约2.3 g/cm3)大于熔融的冰晶石(大约2.1 g/cm3)。于是在高温下,铝会沉积在电解池的底部,通过虹吸原理从电解池中移出。移除铝的同时,加入氧化铝以维持生产[8]。
合理设计的电解池可以通过磁流体动力学进行搅拌。
铝的化合物
氢氧化铝
氢氧化铝不稳定:
\ce{2Al(OH)3 ->[\triangle] Al2O3 + 3H2O}
氢氧化铝有两种电离方式:
氢氧化铝的碱式电离:\ce{Al(OH)3 <=> Al^3+ + 3OH-}。
氢氧化铝的酸式电离:\ce{Al(OH)3 + H2O <=> [Al(OH)4]- + H+}。
实验室制取氢氧化铝:
\ce{Al^3+ + 3NH3*H2O -> Al(OH)3 v + 3NH4+}。
\ce{[Al(OH)4]- + CO2 -> Al(OH)3 v + HCO3-}。
\ce{Al^3+ + 3[Al(OH)4]- -> 4Al(OH)3 v}。
容易想到,对于 \pu{1mol} 铝单质,我们用 \pu{3mol} 氢离子将其转化为 \pu{1mol} 铝离子,然后用 \pu{3mol} 氢氧根将其转化为氢氧化铝。但是这很费原料,不妨进行改进:先用水和 \pu{1mol} 氢氧根转化为四羟基合铝离子,然后用 \pu{1mol} 氢离子转化为氢氧化铝。但是我们还有更好的方法:
将 4\op{mol} 铝单质分为两份,一份 3\op{mol} 用 3\op{mol} 氢氧根处理为四羟基合铝离子,一份 1\op{mol} 用 3\op{mol} 氢离子处理为铝离子,两份混合得到 4\op{mol} 氢氧化铝。相当于 1\op{mol} 铝消耗 3/4\op{mol} 氢离子和氢氧根。
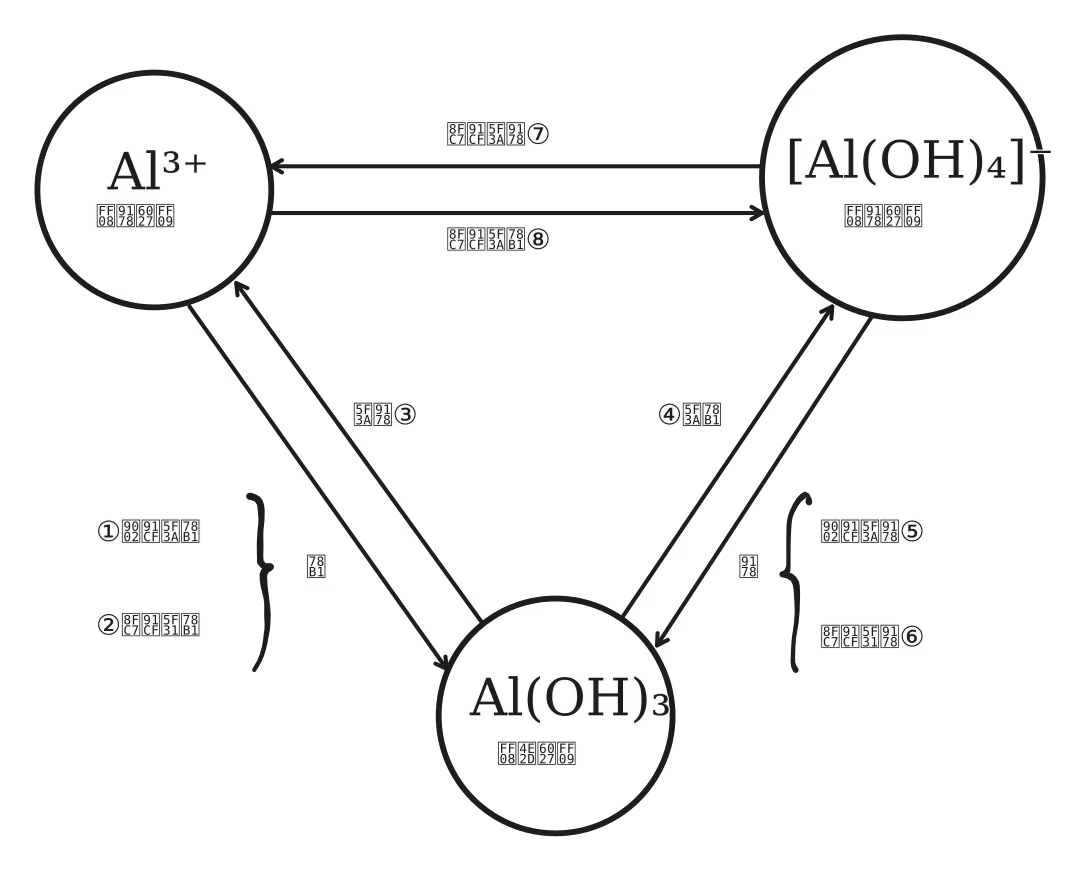
铝三角
| 编号 | 反应方程式 |
|---|---|
| ① | \ce{Al^3+ + 3OH- -> Al(OH)3 v} |
| ② | \ce{Al^3+ + 3NH3*H2O -> Al(OH)3 v + 3NH4+} |
| ③ | \ce{Al(OH)3 + 3H+ -> Al^3+ + 3H2O} |
| ④ | \ce{Al(OH)3 + OH- -> [Al(OH)4]-} |
| ⑤ | \ce{[Al(OH)4]- + H+ -> Al(OH)3 v + H2O} |
| ⑥ | \ce{[Al(OH)4]- + CO2 -> Al(OH)3 v + HCO3-} |
| ⑦ | \ce{[Al(OH)4]- + 4H+ -> Al^3+ + 4H2O} |
| ⑧ | \ce{Al^3+ + 4OH- -> [Al(OH)4]-} |
三氧化二铝
熔点高,不易熔化,故常用作耐火材料。
铝热反应
铝热反应是一种利用铝的强还原性,通过剧烈放热(温度可达2500–3000℃)还原金属氧化物的方法,尤其适用于高熔点金属的冶炼。
- 钒(V):通过铝粉与五氧化二钒(V₂O₅)反应生成金属钒。
- 铬(Cr):铝还原三氧化二铬(Cr₂O₃)生成金属铬。
- 锰(Mn):铝还原二氧化锰(MnO₂)生成金属锰。
- 铁(Fe):铝热法常用于生产低碳或无碳铁合金(如高钒铁合金)。
- 钛(Ti):铝热反应可制备钛铝合金(TiAl₃),用于航空航天材料。